Настольная книга учителя химии 10 класс - поурочные разработки
УГЛЕВОДЫ, ИХ КЛАССИФИКАЦИЯ И ЗНАЧЕНИЕ - УГЛЕВОДЫ
Цели урока. Дать общее понятие об углеводах, как о полифункциональных органических соединениях. Рассмотреть классификацию углеводов по различным признакам. Показать значение отдельных представителей этого типа соединений.
Оборудование: глюкоза (кристаллическая и раствор), сахароза, растворы AgNO3, NH3, Na2CO3, CuSО4, NaOH; спиртовой раствор резорцина (или тимола или α-нафтола), H2SО4 (конц.).
I. Общее представление об углеводах
Первый урок по углеводам методически достаточно сложен. Для формирования у школьников представления об отличительных признаках строения молекул, полноценной классификации этого типа соединений необходимо знать структурные особенности углеводов, а это материал следующих уроков. Получается некий замкнутый круг. Для того чтобы с меньшими потерями пройти этот участок пути, учитель в качестве предшествующего уроку домашнего задания просит ребят повторить первоначальные сведения об углеводах, полученные в курсе химии 9-го класса. Кроме того, последующая классификация углеводов должна носить некоторый декларативный характер. Отнесение углеводов к различным типам закрепляется на последующих уроках параллельно с изучением их структуры и химических свойств.
Углеводы являются, пожалуй, первым из изучаемых классов природных веществ, столь распространенных в природе и хорошо известных каждому ребенку. Вместе с тем это уже достаточно сложные полифункциональные соединения с громоздкими формулами, требующими не только понимания, но и запоминания. Отсюда вывод: к изучению углеводов ребятам следует подойти с должным вниманием и ответственностью.
Тростниковый сахар был известен людям достаточно давно. Родиной сахарного тростника считается Индия. В соке этого растения содержится углевод сахароза, который мы привычно называем сахаром. Белые твердые куски, похожие на камни, использовали не только для придания сладкого вкуса пище, но и как лекарственное средство. В XII в. сахарный тростник стали возделывать на Сицилии, а в XVI в. он был завезен на Кубу и другие острова Карибского моря. Примерно в то же время сахарозу стали завозить в Европу.
«Главной сладостью» в европейских государствах с давних времен был мёд и продукты на его основе. На первых порах сахар был заморской диковинкой и непозволительной роскошью. Потребность в новом продукте резко возросла, когда в европейских странах в моду вошли чай и кофе. Естественно, стали предприниматься многочисленные попытки получения сахара из растений, произрастающих в более холодных климатических условиях Европы. Производство сахара из свеклы связано с именем Андреаса Сигизмунда Марграффа, немецкого химика и металлурга. Марграфф одним из первых применил в химических исследованиях микроскоп, с помощью которого и обнаружил в 1747 г. кристаллы сахара в свекольном соке.
К середине XIX в. химикам было известно уже около десятка веществ, обладающих схожими с сахарозой свойствами. Из сладких плодов и ягод был выделен виноградный сахар, названный в последствии глюкозой. В составе мёда обнаружен углевод, очень похожий на глюкозу, но в отличие от нее очень трудно кристаллизующийся. Его назвали плодовым сахаром, теперь химики называют его фруктозой. Из молока млекопитающих еще в XVII в. был получен кристаллический молочный сахар (лактоза).
Несмотря на столь разные источники получения углеводов, различную степень их сладости, химики с удивлением констатировали, что состав всех этих веществ мог быть выражен формулой Cn(H2O)m. Это и послужило появлению исторически сложившегося названия подобных веществ — углеводы. Учитель отмечает, что современное понятие углеводов основано не на формальном соответствии состава приведенной выше формулы, а сходстве химического строения и свойств веществ этого класса. Поэтому состав некоторых углеводов не соответствует формуле Cn(H2O)m, и наоборот, многие вещества с подобным составом не являются углеводами.
Перед тем как провести классификацию углеводов, необходимо в общих чертах выяснить природу содержащихся в их молекулах функциональных групп. Из курса химии 9-го класса школьникам известна молекулярная формула глюкозы: C6H12O6. Следовательно, глюкоза относится к кислородсодержащим органическим веществам. В состав каких функциональных групп входит атом кислорода? Учащиеся называют гидроксильную, карбонильную, карбоксильную группы. Как правило, до простых и сложных эфиров дело не доходит. Но атомов кислорода в молекуле шесть, значит, кислородсодержащих функциональных групп в молекуле несколько.
Имея в распоряжении водный раствор глюкозы, учитель с помощью качественных реакций проверяет наличие в молекуле различных функциональных групп. Данный эксперимент целесообразно провести на этом уроке еще и потому, что занятие по моносахаридам значительно более насыщено информацией.
1. Прежде всего, хорошая растворимость углеводов в воде позволяет предположить наличие в их молекулах нескольких полярных функциональных групп.
2. Каким образом можно определить наличие в молекуле карбоксильной группы? Водный раствор глюкозы имеет нейтральную реакцию на индикатор, не взаимодействует с раствором карбоната натрия. Следовательно, карбоксильной группы в молекуле глюкозы нет.
3. Учитель спрашивает класс, с помощью каких реакций можно определить в молекуле альдегидную группу. Одни из таких тестов — реакция «серебряного зеркала». Она дает с глюкозой положительный результат — этот углевод является альдегидом.
4. В молекуле глюкозы шесть атомов кислорода. Могут ли все они быть в составе альдегидных групп? Нет, поскольку альдегидная группа может располагаться только на концах углеродной цепи. Тогда, быть может, это поликетон? Тоже исключено: в молекуле содержится 12 водородных атомов. Предположим, в молекуле глюкозы несколько гидроксильных групп. Какую качественную реакцию на многоатомные спирты могут вспомнить ребята? Образование ярко-синих комплексных соединений с гидроксидом меди (II). Демонстрация наглядно показывает, что глюкозу действительно можно отнести к многоатомным спиртам.
Таким образом, не записывая уравнения реакций, совместными усилиями учитель с ребятами пришли к выводу, что простейшие углеводы — это полифункциональные соединения. В их составе содержится карбонильная группа и несколько гидроксильных.
В органическом анализе есть одна замечательная качественная реакция на углеводы. В нее вступают любые сахара: моно-, олиго- и полисахариды, растворимые и нерастворимые в воде, альдозы и кетозы, восстанавливающие и невосстанавливающие. Эта реакция называется пробой Молиша. Если в распоряжении учителя есть спиртовой раствор какого-либо из перечисленных ароматических гидрокси- соединений (резорцин, тимол, α-нафтол), он сумеет показать детям эту красивую реакцию.
В чисто вымытую пробирку наливают 1 мл воды и добавляют несколько крупинок сахарозы, или кристалликов глюкозы, или кусочек фильтровальной бумаги (целлюлоза). В раствор добавляют
2-3 капли раствора резорцина. Пробирку закрепляют в штативе наклонно и по стенке осторожно наливают 1-2 мл концентрированной серной кислоты. Пробирку поворачивают в вертикальное положение. В месте соприкосновения серной кислоты с водным раствором появляется красивое ярко-красное кольцо, свидетельствующее о наличие в исследуемой пробе углевода.
II. Классификация углеводов
Классификация углеводов сложна и многопланова, поскольку проводится по большому числу признаков. Для большей наглядности учитель использует схему, изображенную на рисунке 33. Ребята перерисовывают ее в тетрадь и возвращаются к ней по мере изучения новых типов углеводов. В схеме приведена классификация углеводов по числу остатков моносахаридов в молекуле, по числу углеродных атомов в моносахариде и природе карбонильной группы в нем, по отношению к окислителям.
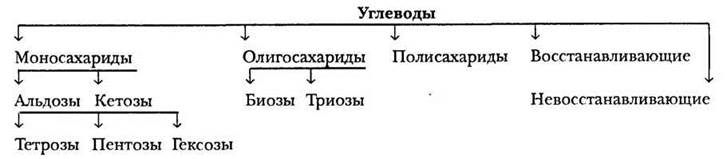
Рис. 33. Классификация углеводов
Углеводы, которые нельзя превратить гидролизом в более простое соединение, называются моносахаридами. Если углевод содержит несколько (от двух до десяти) остатков моносахаридов и образует их при гидролизе, его называют олигосахаридом. Полисахариды представляют собой природные полимеры, состоящие из нескольких сотен и даже тысяч остатков моносахаридов.
Если моносахарид содержит альдегидную группу и представляет собой альдегидоспирт, его называют альдозой. Если карбонильная группа находится не у первого углеродного атома, углевод является кетоспиртом и называется кетозой. По числу углеродных атомов в молекуле моносахариды делятся на тетрозы (4 атома С), пентозы (5), гексозы (6) и т. д. В природе чаще всего встречаются пентозы и гексозы.
Олигосахариды, способные вступать в реакцию с реактивом Толенса (реакция «серебряного зеркала»), называются восстанавливающими, в противном случае — невосстанавливающими.
Задание 1
1-й уровень
Даже великие химики нередко ошибались. Одним из первых определил элементный состав сахарозы А. Л. Лавуазье и получил следующие результаты: углерод — 28%, водород — 8%, кислород — 64%., Вычислите действительное содержание этих элементов в сахарозе, зная ее молекулярную формулу С12Н22О11.
2-й уровень
Можно ли по данным элементного анализа (массовым долям: элементов) различить глюкозу С6Н12О6 и рибозу С5Н10О5. Почему?
Задание 2
1-й уровень
При нуле градусов Цельсия в 100 г воды растворяется 179 г сахарозы или 32 г глюкозы. Рассчитайте массовую долю этих углеводов; в насыщенных растворах при данной температуре.
2-й уровен.
В среднем сладкоежки кладут 2 чайные ложки сахара на стакану чая. Зная, что в такой ложке помещается 7 г сахара, а объем стакана 200 мл, рассчитайте массовую долю сахарозы в растворе (плотность чая считать равной 1 г/мл).